5) ENSEMENCEMENT
5.1) Quelle souche de spiruline utiliser ?
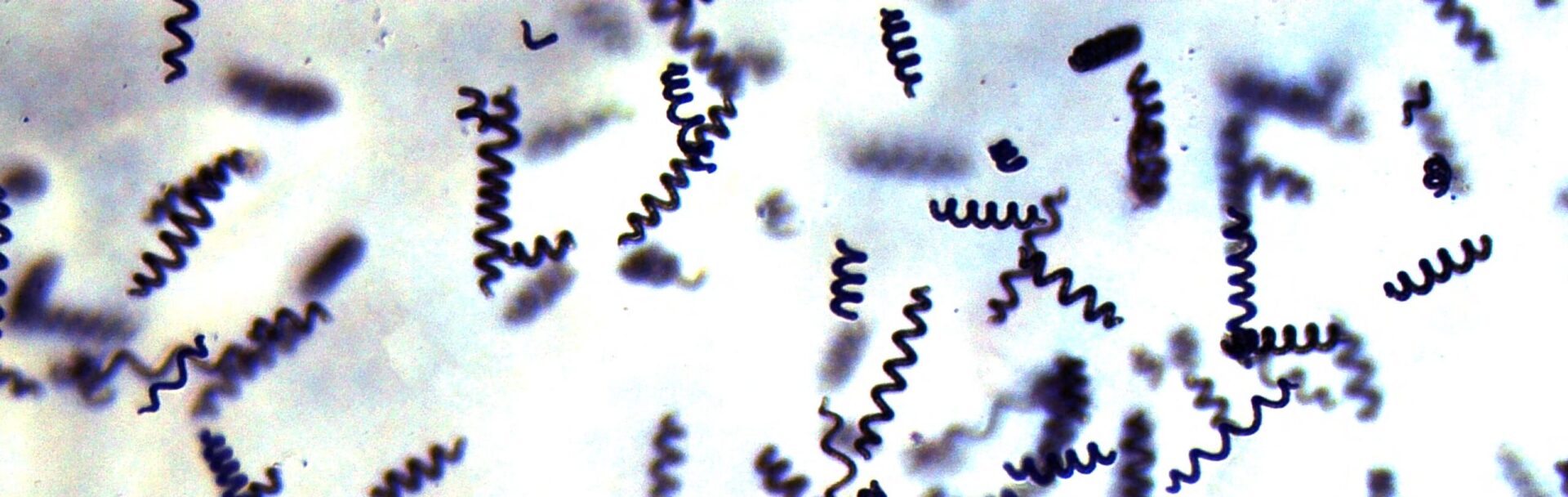
Il existe des spirulines de « races » (souches) différentes, bien qu’elles aient toutes des caractères communs qui les distinguent des autres cyanobactéries. On reconnaît très vite au microscope ou même à la loupe de fort grossissement (25 fois) si les spirulines sont spiralées ou droites mais il est moins facile de dire de quelle souche il s’agit car les spirulines ont une forte tendance à changer de taille et de forme (spiralée plus ou moins serrée ou « ondulée » ou droite). En présence de formes droites il existe un doute : s’agit-il de spirulines ou d’Oscillatoria semblables aux spirulines droites et dont certaines sont toxiques ? Un œil exercé ne peut confondre une droite avec une des Oscillatorias toxiques courantes (Cyanobactériess étrangères). Un trop fort pourcentage de droites conduit à des difficultés de récolte. Donc prendre de préférence une semence 100 % spiralée, de grande taille, d’un beau vert tirant vers le bleu-vert, filtrant facilement. On peut se procurer des souches pures à l’Institut Pasteur chez qui la « Lonar » s’appelle PCC 8005, mais Pasteur n’offre plus ce service. Presque toutes nos souches sont en fait des « Arthrospira platensis » selon la dénomination scientifique. Nous appelons « spiralées » type « Lonar » les souches dont les filaments sont en « queue de cochon », telle la « Lonar ». Nous appelons « spiralées ondulées » (ou « ondulées » tout court) les souches dont les filaments sont en spirale étirée, telle la « Paracas ». Pour faciliter le choix de la souche, voici quelques éléments utiles :
– Les spiralées type Lonar flottent en général plus que les ondulées et les droites, ce qui permet éventuellement leur séparation.
– Les spiralées filtrent mieux et leur biomasse fait la boule facilement sur le filtre, du moins lorsque le milieu de culture est assez pur.
– Les spiralées ont plus tendance à former des peaux et grumeaux verts flottants, surtout à pH bas et en l’absence d’ammonium (voir § 7.9), ce qui est un inconvénient.
– La teneur en matière sèche dans la biomasse essorée prête au séchage est plus élevée chez les ondulées et les droites que chez les spiralées type Lonar, ce qui est un avantage.
– La biomasse des spiralées type Lonar sèche plus facilement.
– Les ondulées n’ont pratiquement pas tendance à devenir droites, du moins dans les conditions d’exploitation normales.
– Les ondulées résistent au pompage par pompe centrifuge, alors que les spiralées se cassent.
– Les ondulées résistent mieux au choc osmotique (on peut parfois laver la biomasse avec de l’eau douce sans que les cellules n’éclatent, alors qu’avec les ondulées c’est rare).
Il n’y a pas de différences de composition ou de valeur nutritionnelle notables entre ces souches, par contre la couleur verte des ondulées est plus sombre ; certains préfèrent la couleur et la saveur de l’une ou l’autre souche, mais ceci est affaire de goût personnel.
Les ondulées et les droites ont des caractères communs, mais les ondulées ne souffrent pas de la suspicion de ne pas être de « vraies » spirulines.
Au total, notre préférence pratique va aux « ondulées », bien que les « spiralées » soient plus belles d’aspect au microscope.
5.2) Ensemencement à partir d’une quantité importante de semence
Pour ensemencer il suffit de transvaser dans du milieu de culture neuf un certain volume de culture provenant d’un autre bassin en production jusqu’à ce que la couleur devienne verte (le « disque de Secchi » ne doit plus se voir à 5 cm de la surface). On ensemence de préférence le soir. On peut réduire le volume à transférer en prélevant du surnageant concentré ou encore en récoltant de la spiruline sans l’essorer (bien la disperser dans un peu de milieu de culture avant de la verser dans le bassin, ceci pour éviter de laisser des grumeaux, ce qui n’est pas facile avec les souches spiralées : utiliser par exemple une hélice de mélangeur de peintures branchée sur une perceuse).
Pour réussir le démarrage d’une culture, on a toujours intérêt à démarrer aussi concentré que possible en spiruline. C’est pourquoi on démarre avec le niveau minimum de liquide (par exemple 5 à 10 cm) si la disponibilité de semence est limitée, et/ou on utilise la technique du « bassin à géométrie variable ». Une culture ensemencée concentrée (Secchi < 3 par exemple) risque beaucoup moins d’être envahie par les chlorelles ou de souffrir de l’entraînement de spirulines dans les boues calcaires (quand on travaille avec une eau dure).
Si la culture commençante est trop diluée (« Secchi » supérieur à 5 cm), il faut ombrer, sinon on risque la mort des spirulines par photoxydation au soleil. Il faut aussi veiller à éviter les dépôts minéraux qui entraînent avec eux des spirulines (pour cela filtrer au besoin le milieu neuf avant de l’ensemencer et maintenir l’agitation pendant la nuit si possible). Si le niveau initial est le niveau normal, et si le milieu neuf est à base de bicarbonate de sodium, ne pas ensemencer trop concentré non plus, sinon il faudra récolter avant que le pH ait atteint le niveau minimum de 9,6 recommandé (voir § 7.13) ; mais il est facile de démarrer avec un milieu de culture à pH 9,6 ou plus en mélangeant au bicarbonate de sodium du carbonate de sodium ou de la soude (voir Annexe 12 et Annexe 13). Un autre avantage d’un pH initial élevé est la réduction de la tendance initiale à la formation de grumeaux avec les souches spiralées, avantage pouvant être décisif quand on a peu de semence : il ne faut pas en perdre en grumeaux ! D’autre part il est certain qu’il y a intérêt à ne pas soumettre la semence de spiruline à un choc de pH : il nous est arrivé de voir mourir une culture débutante suite à un choc de pH de 2 unités (de 10 à 8) : notre recommandation est de limiter le delta Ph à 1 unité.
Il est permis de stocker quelques jours et transporter une semence très concentrée (3 à 4 g/l par exemple, pas plus), à condition de l’agiter et de l’aérer au moins de temps à autre sinon elle fermente et sent mauvais. A 2 g/l, le transport peut durer dix jours. A noter qu’une couche flottante prélevée avec soin peut tirer 5 à 10 g/l. Dans une semence très concentrée le pH baisse et une odeur mercaptée (odeur de « choucroute ») se développe au cours du temps. Après l’ensemencement avec une spiruline ayant « souffert » au stockage, le nouveau bassin peut mousser excessivement, mais cela disparaît normalement en un à deux jours.
La semence se conserve mieux à basse température, vers 10°C par exemple (réduction de la respiration). La biomasse fraîche, même pressée, peut servir à ensemencer un bassin. C’est important pour faciliter le transport sous forme concentrée et pour ensemencer immédiatement un grand volume. Faire le transport à froid autant que possible, et en limiter la durée. Diluer progressivement la semence concentrée, en l’homogénéisant : il ne doit pas rester de grumeaux (passer le mélange sur tamis pour éliminer les éventuels grumeaux restant).
5.3) A partir d’une petite quantité de semence
Pour implanter une culture de spiruline dans un site qui en est dépourvu, ou pour redémarrer avec une nouvelle souche, il n’est généralement pas possible de disposer d’une grande quantité de culture pour ensemencer. Fréquemment on ne dispose que d’un flacon rempli à moitié seulement (pour maintenir assez d’oxygène). Si on réussit à se procurer une souche pure, on n’aura probablement que quelques millilitres de culture au départ (N.B. le milieu de culture indiqué par l’Institut Pasteur dans sa documentation accompagnant ses souches correspondait au maintien des souches et il diffère du milieu de culture pour la croissance). On peut aussi partir d’un seul filament qu’on isole soi-même (voir § 5.6).
Supposons que le point de départ soit 150 g de culture à 1 g/l de concentration en spiruline et que l’objectif soit de multiplier le volume de semence initial pour ensemencer un bassin de 1000 litres. Il va falloir faire au moins 4 cultures successives, en multipliant chaque fois le volume par 5, ce qui demande environ trois semaines au total (avec un taux de croissance de 35 %/jour, possible avec du milieu de culture à base de bicarbonate de sodium). La première mini-culture se fera dans un bocal de deux litres, la seconde dans une bassine de 10 litres, la troisième dans une bassine de 50 litres, la dernière dans un mini bassin provisoire en film plastique de 1 m² (ou plusieurs grandes bassines).
Si la concentration initiale de chaque culture est plus faible que Secchi = 5 cm, il faut non seulement ombrer mais agiter jour et nuit (sinon les spirulines peuvent s’agglomérer, notamment sur les bords, et ne plus pouvoir se disperser ensuite). Il est possible d’éviter cette agglomération en relevant le pH, mais cela risque d’augmente les boues minérales qui peuvent piéger les spirulines. Moyennant quoi on arrive quand même à démarrer une culture en partant de très faibles concentrations (Secchi = 15).
L’agitation continue des cultures en petits récipients (bouteilles, seaux, bassines par exemple) se fait au moyen d’un petit bullage d’air comme dans un aquarium et nécessite un rapport hauteur de liquide/diamètre élevé, égal ou supérieur à 1, avec si possible un fond conique, le tube d’amenée d’air débouchant tout près du fond (il existe des compresseurs d’aquarium fonctionnant sur pile électrique). Il est pratique de chauffer et éclairer simultanément les petites cultures initiales en laboratoire par des lampes à incandescence ou halogène placées à la bonne distance pour maintenir automatiquement environ 35°C dans la culture (ne pas éclairer plus de 16 hr/jour).
L’agitation de volumes importants (> 100 litres) de cultures diluées peut se faire au moyen d’une petite pompe d’aquarium, mais on a intérêt à ne pomper que par intermittance pour ne pas abîmer les spirulines, surtout les Lonar,, les souches ondulées sont beaucoup moins sensibles aux dégâts des pompes.
Pour éviter la formation de grumeaux (surtout avec les souches spiralées type Lonar et s’il n’y a pas d’agitation continue) au début de l’ensemencement, il faut diluer très progressivement la semence concentrée, en ajoutant des petites doses de milieu de culture neuf à base d’urée, par exemple à chaque agitation, en gardant une concentration élevée en spirulines les deux premiers jours. On a ensuite intérêt à conserver une concentration en spiruline élevée (0,3 g/l ou plus) et donc à diluer le moins possible la culture à chaque augmentation de volume : une dilution progressive (par exemple quotidienne) est la meilleure. On peut pour cela utiliser un « bassin à géométrie variable », extensible en surface, facile à réaliser avec du film plastique. Chaque augmentation de volume (donc surface) se fait par dilution à l’aide de milieu de culture neuf (de préférence à base de bicarbonate de sodium). Le milieu de dilution – s’il est à base d’urée comme source d’azote – doit comporter une forte dose d’urée (0,04 g/l) ou, s’il est à base d’urine : 6 ml d’urine/l. Si le milieu neuf est à base de bicarbonate de sodium, donc de pH = 8, le pH de la culture se maintient autour de 9,6 pendant sa phase d’extension. Ce pH peut ne pas être suffisant pour éviter les grumeaux de spiralées : dans ce cas relever le pH en ajoutant du milieu à base de carbonate jusqu’à pH = 10,3. On accélère la croissance pendant la phase « bassin à géométrie variable » en maintenant la profondeur faible (5-10 cm).
N.B. :
1) Une culture peut mourir suite à une dilution, un éclairage ou un chauffage trop forts ou un excès d’urée.
2) L’augmentation de niveau d’un bassin doit se faire par ajout de milieu de culture. L’ajout directement dans le bassin des sels non dissous peut être très dangereux pour la culture.
3) Si on prépare d’avance une réserve de milieu de culture de dilution, la garder peu de temps et fermée et à l’obscurité pour qu’elle ne risque pas de se contaminer par des algues étrangères.
4) Attention : un choc de pH de 2 unités est souvent mortel : lors des ensemencements veillez à minimiser les différences de pH entre semence et bassin.
5.4) Taux de croissance initial
La vitesse de croissance dépend de plusieurs facteurs dont le pH. Elle est maximum à pH inférieur à 10, donc on a intérêt à utiliser le bicarbonate de sodium pour démarrer rapidement une nouvelle culture. On a aussi intérêt à maximiser la surface de culture (donc bassin peu profond si possible). La méthode d’extension progressive de la surface de bassin (« à géométrie variable ») décrite au § précédent favorise une croissance rapide. On caractérise au mieux la rapidité d’implantation d’une nouvelle culture en calculant le taux de croissance dans la phase initiale de croissance qui précède la phase des récoltes. Ce taux s’exprime en % de croissance en poids par jour poids exprimé en sec). Dans des conditions favorables, en milieu à base de bicarbonate de sodium, il peut dépasser 30%/jour. A partir d’un gramme de semence (exprimé en spiruline sèche), un taux de 20%/jour permet d’obtenir 20 m² de bassin de 15 cm de profondeur prête à la récolte en 40 jours, ou 120 m² en 50 jours.
N.B. On serait tenté d’éclairer les cultures 24 heures par jour pour augmenter le taux de croissance, mais il vaut mieux ne pas soumettre les spirulines à plus de 16 heures d’éclairement par jour, même si l’on dispose d’éclairage artificiel.
5.5) Réserve de semence
En temps normal les bassins eux-mêmes servent de réserve s’ils restent en bonne santé et sans contaminant, mais il faut prévoir les accidents et comment passer la mauvaise saison éventuelle. On a aussi intérêt, quand on le peut, à vidanger complètement les bassins et à les redémarrer à zéro pour assurer le maintien d’une bonne qualité de spiruline (sans contaminant, sans droites, filtrant bien). Pour cela il faut disposer de semence pure. Il est donc recommandé de conserver un peu de souche pure « en laboratoire » (= dans la maison), à température modérée ou ambiante, sous faible éclairage environ 12 heures/jour (en l’absence totale de lumière la spiruline meurt en quelques jours, par exemple en 2 jours à 35°C), légèrement agitée, et renouvelée (« repiquée ») tous les 2 ou 3 mois : dans ces conditions, elle se conserve bien alors qu’une température trop intensive elle a tendance à muter et peut dégénérer. Une bouteille en plastique convient très bien comme récipient. Pour agiter et aérer, le plus pratique est un petit compresseur d’air électrique pour aquarium, qu’on peut ne faire marcher que de temps en temps grâce à un programmateur (il existe de tels compresseurs et programmateurs fonctionnant sur courant continu). Pour à la fois éclairer et chauffer la culture il suffit d’une lampe de chevet de 40 Watt dirigée horizontalement vers la bouteille, à la distance donnant une température correcte (< 30°C). Pour conserver des quantités plus importantes de semence, on utilise des bassines ou aquariums, avec des lampes plus puissantes, à incandescence ou halogènes ; les tubes luminescents chauffent peu et conviennent si la température ambiante est suffisamment élevée. Photo d’une réserve de semence :
5.6) Sélection et culture monoclonale
L’ensemencement à partir de n’importe quelle semence donne une culture ayant les mêmes contaminants éventuels que la semence. Pour être sûr d’avoir une culture pure (« monoclonale »), il faut théoriquement partir d’un seul filament sélectionné et lavé avec du milieu stérile.
Il est possible de séparer un filament individuel à partir d’un mélange de souches. Diverses techniques, basées sur une dilution de la culture d’origine, sont utilisables pour effectuer cette séparation, qui reste une opération difficile pour un non-spécialiste.
Il est plus facile et rapide de prélever dans une culture très peu contaminée (par des spirulines droites par exemple) une goutte sans contaminant : la sélection se fait par examen au microscope à faible grossissement, en rejetant les gouttes contaminées ne serait-ce que par un seul filament étranger et en mettant les gouttes pures dans du milieu de culture filtré (en rinçant la lame de microscope à la pissette remplie de milieu de culture filtré). On collecte autant de « gouttes » pures que l’on peut dans le temps disponible : plus il y en aura, plus vite on obtiendra une semence utilisable. Il est prudent de faire cette opération de sélection régulièrement pour maintenir ainsi un stock pur de sécurité sans attendre qu’un % de contaminants (droites par exemple) trop élevé rende l’opération de sélection difficile.
5.7) Dérive d’une culture vers une autre souche
Il est fréquent d’assister en cours de culture à une variation de forme et/ou de taille des filaments de spiruline. Vers la forme droite bien sûr mais aussi vers d’autres formes spiralées, notamment vers des formes plus petites ou resserrées qui passent préférentiellement dans le filtrat. Il serait illusoire de chercher à contrer cette dérive par l’utilisation de toiles de filtration à maille plus fine (ce qui ne fait en général que ralentir l’évolution). La seule parade radicale, en dehors de la purge, est le non recyclage direct des filtrats : le recyclage doit se faire à travers le système d’épuration (Epuration).