SOMMAIRE DES ANNEXES
A1) Influence de différents facteurs sur la croissance
A2) Mesure de la concentration en spiruline
A3) Mesure de la salinité
A4) Mesure du pH
A5) Mesure de l’alcalinité
A6) Tests de qualité faciles à réaliser
A7) Absorption du CO2 atmosphérique
A8) Interaction Photosynthèse/Absorption du CO2
A9) Productivité en fonction de l’ombrage
A10) Consommation d’eau en fonction de l’ombrage
A11) Correspondance entre pH et rapport CO2/base
A12) Mélanges de carbonate et de bicarbonate de sodium
A13) Neutralisation de l’eau de cendre
A14) Composition de divers produits
A15) Matériel de laboratoire utile
A16) Produits chimiques
A17) Normes de la spiruline
A18) Limites de concentrations dans le milieu de culture
A19) Composition élémentaire de la spiruline
A20) Composition nutritionnelle de la spiruline
A21) Éléments de prix de revient et fournisseurs
A22) Pour comparer les spirulines à d’autres algues
A23) Spirulines vues au microscope
A24) Pour ceux qui ont de l’électricité
A25) Hivernage
A26) Formules d’Oligo-éléments
A27) Modèles de Séchoirs
A28) Projet semi-artisanal de 5 kg/jour
A29) Check list pour démarrage de spiruline
A30) Spiruline humanitaire dans les PVD (par P. Ancel, mai 2004)
A31) Adoucissement de l’eau
A1) Influence de différents facteurs sur la croissance
Nous présentons ici des courbes de croissance obtenues à partir de mesures de densité optique. La première série de graphiques (fig. A1) montre l’effet de différentes concentrations en nutriments.

A2) Mesure de la concentration en spiruline
1) Avec spectrophotomètre (méthode la plus fiable)
La mesure de densité optique (OD) à 680 nm permet une évaluation directe de la concentration en spiruline. Cette méthode est très largement utilisée dans la recherche et l’industrie.
Relation OD / concentration :
Une OD de 1.0 à 680 nm correspond à environ 0.5 g/L de spiruline sèche.
Protocole simplifié :
1. Remplir une cuve de 1 cm d’épaisseur avec le milieu de culture sans spiruline
2. Faire un blanc avec ce milieu
3. Remplir une cuve avec une dilution de la culture à mesurer
4. Mesurer l’OD à 680 nm
5. Multiplier l’OD mesurée par le facteur de dilution
6. Multiplier par 0.5 pour obtenir la concentration en g/L
2) Mesure du poids sec
C’est la méthode de référence.
Protocole :
1. Peser un filtre sec (m1)
2. Filtrer un volume connu de culture (ex : 100 mL)
3. Rincer le filtre avec de l’eau distillée
4. Sécher le filtre à 105°C jusqu’à poids constant (au moins 2 heures)
5. Peser le filtre + spiruline (m2)
6. Concentration = (m2 – m1) / volume filtré * 1000
3) Estimation visuelle
Pour une évaluation rapide en terrain :
– Très dilué (vert clair) : 0,1 à 0,3 g/L
– Dilué (vert) : 0,3 à 0,7 g/L
– Normal (vert-bleu) : 0,7 à 2 g/L
– Concentré (bleu-vert) : 2 à 5 g/L
– Très concentré (bleu) : > 5 g/L
A3) Mesure de la salinité
Avec un réfractomètre :
Le réfractomètre est l’outil idéal pour mesurer rapidement la salinité en terrain.
Protocole :
1. Nettoyer le réfractomètre avec un chiffon doux
2. Placer une goutte de solution à mesurer sur la vitre inférieure
3. Fermer le couvercle
4. Observer l’échelle à travers l’oculaire et lire la valeur de salinité
5. La limite bleu-blanc donne directement la salinité en %
Etalonnage :
– Avant chaque utilisation, tester avec de l’eau pure (0%)
– Corriger si nécessaire avec la vis de calibration
A4) Mesure du pH
Avec un pH-mètre électronique :
Protocole :
1. Rincer les électrodes avec de l’eau distillée
2. Étalonner l’appareil avec des solutions tampon (pH 7 et pH 9 ou 10)
3. Rincer les électrodes
4. Immerger les électrodes dans l’échantillon à mesurer
5. Attendre la stabilisation (30 secondes environ)
6. Lire la valeur
Avec du papier pH :
Moins précis mais utile en terrain :
1. Tremper une bande de papier pH dans l’échantillon
2. Comparer la couleur avec l’échelle fournie
3. Lire la valeur
A5) Mesure de l’alcalinité
Titrage à l’acide chlorhydrique :
C’est la méthode la plus précise pour mesurer l’alcalinité.
Protocole :
1. Prélever 50 mL de culture
2. Ajouter 3 gouttes de phénolphtaléine
3. Si la couleur devient rose/rouge :
- Titrer avec HCl 0,1 N jusqu’à disparition de la couleur rose (V1)
4. Ajouter 3 gouttes de méthyle orange
5. Titrer avec HCl 0,1 N jusqu’à virage du jaune à l’orange (V2)
Calculs :
– Alcalinité totale = (V1 + V2) * N * 50 meq/L
– Ou en g/L de CaCO3 : (V1 + V2) * N * 2,5 g/L
où N est la normalité de l’acide utilisé
A6) Tests de qualité faciles à réaliser
1) Test de pureté visuels
Observer au microscope :
– Les filaments doivent tous être spiralés
– Pas d’algues vertes visibles
– Pas de bactéries ou champignons visibles
2) Test de viabilité après séchage
1. Prendre 1 g de spiruline séchée
2. Ajouter 50 mL de milieu Zarrouk dilué de moitié
3. Laisser 24 heures en lumière
4. Vérifier que la culture repart
3) Test de contamination bactérienne
1. Prélever 0,1 mL de culture
2. Diluer en série (10-3, 10-4, 10-5)
3. Verser sur gélose nutritive
4. Incuber 24 heures à 37°C
5. Compter les colonies (ne doit pas dépasser quelques centaines par mL)
4) Test de goût après réhydratation
1. Réhydrater 1 g de spiruline séchée dans 50 mL d’eau
2. Goûter (en petite quantité)
3. Le goût doit être frais, sans saveur « off » ou rancidité
A7) Absorption du CO2 atmosphérique
La spiruline peut absorber directement le CO2 de l’atmosphère. Ceci est particulièrement important dans les systèmes extensifs.
Quantité absorbée :
Sous forme carbonatée, la spiruline contient environ 9% de carbone. Lors de la croissance, la majeure partie du CO2 provient du système tampon (carbonate/bicarbonate) du milieu, mais une part non négligeable peut être absorbée directement de l’air.
Avantages :
– Réduit la dépendance aux apports externes de carbone
– Améliore l’équilibre carbone-azote
– Contribue à réduire le CO2 atmosphérique
A8) Interaction Photosynthèse/Absorption du CO2
L’absorption du CO2 et la photosynthèse sont intimement liées :
Photosynthèse : CO2 + H2O → (CH2O) + O2
Source du CO2 : Milieu de culture (surtout) + absorption atmosphérique (moins)
Taux de photosynthèse :
– Maximale sous lumière optimale
– Dépend de la concentration en CO2 disponible
– Dépend de la température (optimale vers 35-38°C)
– Diminue si la lumière ou le CO2 devient limitant
Rendement énergétique :
L’efficacité photosynthétique dépend du type d’organisme. Les cyanobactéries comme la spiruline ont une efficacité théorique de conversion lumineuse vers biomasse d’environ 5-8%, contre 2-4% pour les plantes supérieures.
A9) Productivité en fonction de l’ombrage
L’ombrage affecte considérablement la productivité :
Productivité (g/m²/jour) :
– Plein soleil (100%) : 7-12 g/m²/jour
– 75% de lumière : 5-9 g/m²/jour
– 50% de lumière : 3-6 g/m²/jour
– 25% de lumière : 1-2 g/m²/jour
– Lumière faible : croissance très réduite
Optimum économique :
Considérant les coûts de climatisation et d’énergie, un ombrage de 20-30% est souvent optimal pour les zones très chaudes.
A10) Consommation d’eau en fonction de l’ombrage
Perte d’eau (évaporation + transpiration) :
– Plein soleil : 10-20 mm/jour
– 50% d’ombrage : 5-10 mm/jour
– 70% d’ombrage : 2-5 mm/jour
Remarques :
– Ces chiffres varient selon le climat local
– L’humidité relative diminue l’évaporation
– La vitesse du vent augmente l’évaporation
– Un ombrage réduit les besoins en eau
A11) Correspondance entre pH et rapport CO2/base
Système tampon du Zarrouk :
Le milieu de culture contient un système tampon carbonate/bicarbonate qui contrôle le pH.
Équilibre chimique :
CO2 + H2O ⇌ H2CO3 ⇌ H+ + HCO3- ⇌ 2H+ + CO3²-
Relation pH / alcalinité :
– pH 8,5 : surtout HCO3- (bicarbonate)
– pH 9,5 : mélange CO3²- / HCO3-
– pH 10,5 : surtout CO3²- (carbonate)
– pH 11 : surtout CO3²- (carbonate)
Pour la spiruline :
L’optimum se situe entre pH 9 et 11, avec une préférence pour pH 10.
A12) Mélanges de carbonate et de bicarbonate de sodium
Pour obtenir un pH spécifique, on peut mélanger Na2CO3 et NaHCO3 dans des proportions différentes :
Pour pH 8,5 : 1 part Na2CO3 + 10 parts NaHCO3
Pour pH 9,0 : 1 part Na2CO3 + 5 parts NaHCO3
Pour pH 9,5 : 1 part Na2CO3 + 2 parts NaHCO3
Pour pH 10,0 : 1 part Na2CO3 + 0,5 parts NaHCO3
Pour pH 10,5 : 1 part Na2CO3 + 0,2 parts NaHCO3
Pour pH 11,0 : Na2CO3 pur
Ces proportions sont approximatives et peuvent varient légèrement selon les conditions locales.
A13) Neutralisation de l’eau de cendre
L’eau de cendre est alcaline (pH élevé) car elle contient des hydroxydes et carbonates de potassium et de sodium.
Pour réduire le pH :
Méthode 1 : par aération
L’aération provoque l’évaporation du CO2, ce qui diminue l’alcalinité et le pH progressivement. C’est la méthode la plus douce.
Méthode 2 : par ajout de CO2
Bubler du CO2 pur (ou de l’air enrichi en CO2) jusqu’à atteindre le pH désiré.
Méthode 3 : dilution
Diluer l’eau de cendre avec de l’eau distillée ou de l’eau de pluie jusqu’à obtenir le pH souhaité.
Méthode 4 : ajout d’acide faible
En dernier recours, on peut ajouter très lentement un acide faible (acide acétique par exemple) en contrôlant bien le pH.
A14) Composition de divers produits
Engrais NPK usuels :
| Produit | N (%) | P (%) | K (%) |
|---|---|---|---|
| Nitrate d’ammonium | 35 | – | – |
| Superphosphate simple | – | 16-20 | – |
| Chlorure de potassium | – | – | 60 |
| Engrais NPK 15-15-15 | 15 | 15 | 15 |
Produits contenant des oligo-éléments :
| Élément | Produit | Pourcentage |
|---|---|---|
| Fer | Sulfate de fer | 20 |
| Magnésium | Sulfate de magnésium (sel d’Epsom) | 10 |
| Manganèse | Sulfate de manganèse | 32 |
| Zinc | Sulfate de zinc | 35 |
| Cuivre | Sulfate de cuivre | 25 |
| Bore | Acide borique | 17 |
A15) Matériel de laboratoire utile
Pour les mesures :
– pH-mètre électronique
– Réfractomètre (pour la salinité)
– Spectrophotomètre (pour concentration en spiruline)
– Thermomètre
– Balance analytique (0,1 g précision)
– Pipettes et burettes
Pour la préparation :
– Béchers
– Fioles jaugées
– Entonnoirs
– Pipette Pasteur
– Baguettes de verre
– Filtres et papier filtre
Pour l’observation :
– Microscope optique
– Lames et lamelles
– Compte-cellules (hémocytomètre)
Pour le travail en culture :
– Autoclave (ou cocotte-minute)
– Érlenmeyers et fioles
– Tubes à essai
– Portoir
– Pipettes stériles
– Boîtes de Pétri
A16) Produits chimiques
Produits pour la préparation du milieu Zarrouk :
| Composant | Formule | Quantité (g/L) |
|---|---|---|
| Nitrate de sodium | NaNO3 | 2,5 |
| Phosphate dibasique de potassium | K2HPO4 | 0,5 |
| Sulfate de potassium | K2SO4 | 1,0 |
| Chlorure de sodium | NaCl | 1,0 |
| Sulfate de magnesium | MgSO4·7H2O | 0,2 |
| Chlorure de calcium | CaCl2·2H2O | 0,04 |
| Chlorure de fer III | FeCl3·6H2O | 0,008 |
| EDTA disodique | Na2EDTA·2H2O | 0,080 |
| Bicarbonate de sodium | NaHCO3 | 16,8 |
| Carbonate de sodium | Na2CO3 | 2,46 |
Oligo-éléments :
Voir annexe A26 pour les formules complètes
A17) Normes de la spiruline
Normes internationales pour la spiruline destinée à la consommation humaine :
Composition nutritionnelle (matière sèche) :
– Protéines : 60-70%
– Lipides : 5-10%
– Glucides : 10-20%
– Minéraux : 5-10%
Teneur en chlorophylle :
– Minimum 0,5% de la matière sèche
Métaux lourds (limites usuelles) :
– Plomb : max 2 mg/kg
– Cadmium : max 0,5 mg/kg
– Arsenic : max 1 mg/kg
– Mercure : max 0,5 mg/kg
Contamination microbienne :
– Coliformes E. coli : < 10 UFC/g
– Staphylococcus aureus : < 1000 UFC/g
– Salmonella : absence dans 25 g
– Listeria monocytogenes : absence dans 25 g
Activité de l’eau (aw) :
– Pour la poudre séchée : aw < 0,65
A18) Limites de concentrations dans le milieu de culture
Concentrations optimales et limites :
| Paramètre | Valeur minimale | Valeur optimale | Valeur maximale |
|---|---|---|---|
| pH | 9,0 | 10,0-10,5 | 11,0 |
| Concentration en spiruline (g/L) | 0,5 | 2,0-4,0 | 8,0 |
| Salinité (%) | 0,5 | 0,8-1,2 | 2,0 |
| Température (°C) | 15 | 35-38 | 42 |
| Azote (mg/L) | 100 | 250-500 | 1000 |
| Phosphore (mg/L) | 20 | 50-100 | 300 |
| Potassium (mg/L) | 100 | 300-600 | 1500 |
| Magnésium (mg/L) | 20 | 50-100 | 500 |
| Fer (µg/L) | 50 | 500-1000 | 5000 |
Remarques importantes :
– Dépassér la concentration limite de spiruline peut provoquer une auto-ombrage excessif
– Une température trop basse ralentit la croissance
– Une salinité trop élevée peut inhiber la croissance
A19) Composition élémentaire de la spiruline
Composition en pourcentage de matière sèche :
| Élément | Pourcentage |
|---|---|
| Carbone (C) | 48-50 |
| Azote (N) | 8-10 |
| Hydrogène (H) | 6-7 |
| Oxygène (O) | 23-25 |
| Phosphore (P) | 0,8-1,0 |
| Soufre (S) | 0,6-0,8 |
| Potassium (K) | 1,0-1,2 |
| Magnésium (Mg) | 0,3-0,5 |
| Calcium (Ca) | 0,2-0,3 |
| Sodium (Na) | 0,5-1,0 |
| Traces (Fe, Mn, Zn, Cu, etc.) | 0,1-0,2 |
A20) Composition nutritionnelle de la spiruline
Composition pour 100 g de spiruline sèche :
| Composant | Quantité | Unité |
|---|---|---|
| Protéines brutes | 60-70 | g |
| Acides gras polyinsaturés | 4,0 | g |
| Glucides disponibles | 10-15 | g |
| Fibres | 3,0 | g |
| Minéraux (cendres) | 7-9 | g |
| Eau (poudre séchée) | 3-5 | g |
| Énergie | 380-390 | kcal |
| Vitamines (pour 10 g) | ||
| Vitamine A (équivalent bêta-carotène) | 4,7 | mg |
| Vitamine E | 1,5 | mg |
| Vitamine B1 (thiamine) | 0,3 | mg |
| Vitamine B2 (riboflavine) | 0,4 | mg |
| Vitamine B3 (niacine) | 1,2 | mg |
| Vitamine B6 | 0,1 | mg |
| Vitamine B12 (cyanocobalamine) | 0,15 | µg |
| Acide folique | 0,035 | mg |
| Minéraux (pour 10 g) | ||
| Calcium | 0,28 | g |
| Phosphore | 0,10 | g |
| Magnésium | 0,04 | g |
| Potassium | 0,15 | g |
| Sodium | 0,06 | g |
| Fer | 3,2 | mg |
| Zinc | 0,4 | mg |
| Manganèse | 0,2 | mg |
| Cuivre | 0,1 | mg |
| Iode | 0,05 | mg |
A21) Éléments de prix de revient et fournisseurs
Coûts de production estimés (en euros, pour une petite production):
| Poste de dépense | Montant annuel estimé | Notes |
|---|---|---|
| Nutriments (sels) | 500-1000 | Pour 2-3 kg de spiruline sèche |
| Eau (si achetée) | 200-500 | Selon zone, peut être gratuit si puits |
| Main-d’œuvre | Variable | Travail quotidien |
| Électricité (pompe, lumière) | 200-500 | Si petit système manuel, 0 |
| Maintenance, remplacement filtres | 100-300 | |
| Transport du produit | Variable |
Fournisseurs typiques (liste non exhaustive) :
Les produits chimiques peuvent être achetés auprès de :
– Distributeurs de produits chimiques locaux
– Pharmacies vétérinaires
– Fournitures agricoles
– Fournisseurs d’aquariophilie
– Fournisseurs industriels en ligne (avec prudence sur la qualité)
A22) Pour comparer les spirulines à d’autres algues
Comparaison de la spiruline avec d’autres micro-algues :
| Caractéristique | Spiruline | Chlorella | Dunaliella | Scenedesmus |
|---|---|---|---|---|
| Type | Cyanobactérie | Algue verte | Algue verte | Algue verte |
| Teneur en protéines (%) | 60-70 | 50-60 | 60-70 | 50-70 |
| Digestibilité | Bonne | Excellente | Bonne | Bonne |
| Coûts de production | Faibles | Moyens | Moyens | Moyens-Élevés |
| pH optimal | 9-11 | 6,5-7,0 | 7,0 | 7,0 |
| Température optimale (°C) | 35-38 | 25-30 | 20-25 | 25-30 |
| Salinité optimale (%) | 0,8-1,2 | 0,5 | 1,5-2,5 | 0,5 |
| Productivité (g/m²/jour) | 5-12 | 3-8 | 2-5 | 3-6 |
| Avantages | Facile, robuste, productif | Haute qualité, digeste | Riche en bêta-carotène | Oméga-3 |
| Inconvénients | Aucun majeur | Coût plus élevé | Moins robuste | Contamination facile |
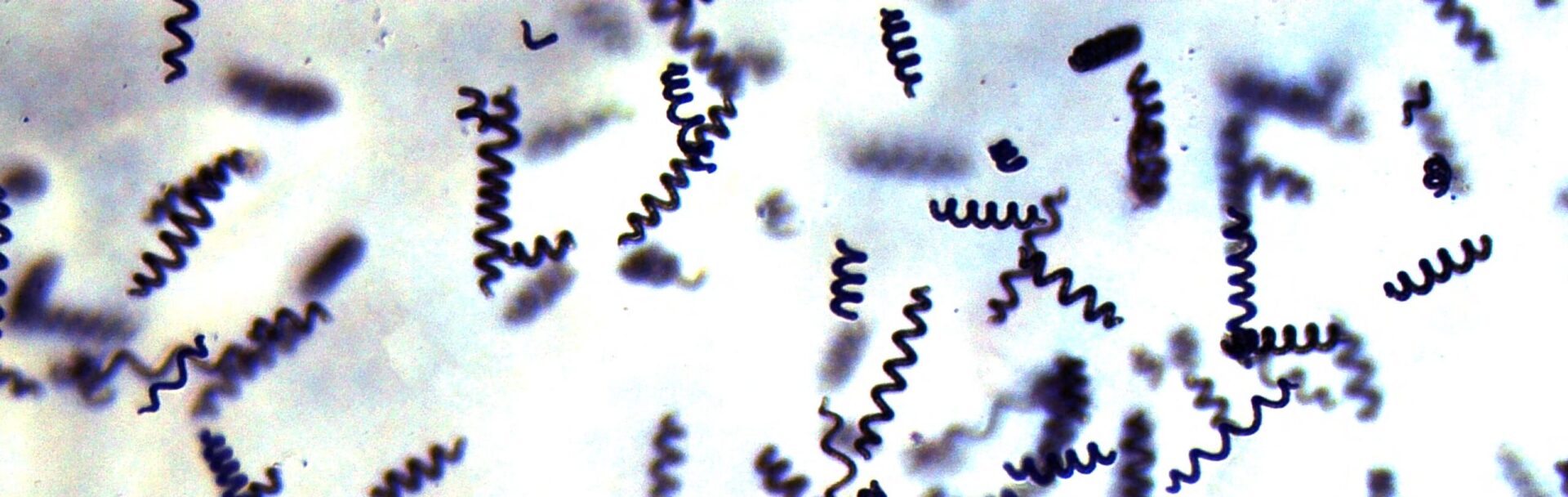
A23) Spirulines vues au microscope
Description morphologique :
La spiruline (*Arthrospira*) est une cyanobactérie filamenteuse qui se présente sous forme de longs filaments hélicoïdaux (en spirale) d’environ 0,5-1 mm de longueur.
Observations au microscope optique :
Grossissement x 40 ou x 100 :
– Filaments hélicoïdaux très caractéristiques
– Couleur bleu-vert due à la phycocyanine
– Cellules bien alignées dans le filament
– Absence de paroi rigide (flexible)
Contaminations visibles au microscope :
– Algues vertes : formes varies, structures différentes
– Bactéries : très petites, mobiles, diverses formes
– Champignons : filaments ramifiés (distincts du spiruline)
– Protozoaires : formes complexes, mobiles, de diverses tailles
– Particules de saleté : amorphes, non pigmentées
Observations de bonne santé :
– Filaments bien alignés et réguliers
– Coloration bleu-vert uniforme
– Absence visible de contaminants
– Mobilité normale du liquide
A24) Pour ceux qui ont de l’électricité
Certains équipements électriques peuvent améliorer la productivité et faciliter la gestion :
Systèmes d’aération :
– Aérateur électrique : apporte CO2 et énergie à l’eau
– Avantages : meilleure croissance, plus de productivité
– Coût : 100-500€ selon taille
– Consommation : 100-500W
Systèmes de chauffage :
– Radiateur électrique ou thermoplongeur
– Utile dans zones froides
– Thermostat recommandé
– Coût : 50-200€
– Consommation : 500-2000W
Éclairage additionnel :
– Lampes LED ou fluorescentes (moins chaudes que l’incandescence)
– Améliore la productivité par mauvais temps
– Coût : 100-300€
– Consommation : 100-200W
Pompes :
– Pour renouvellement d’eau, alimentation, traitement
– Submersibles ou de surface
– Coût : 50-200€
– Consommation : 50-300W
Filtres mécaniques :
– Pour filtration avant récolte
– Électriques ou manuels
– Coût : 100-500€
– Consommation : 50-200W
Règle générale :
Pour une production de 2-5 kg/jour, on n’a pas vraiment besoin d’électricité. Avec électricité, la productivité peut être multipliée par 2-3.
A25) Hivernage
En climat tempéré ou froid, comment conserver la spiruline en hiver :
Méthode 1 : Pause d’hivernage
La spiruline peut supporter plusieurs mois d’hivernage si on la place en conditions minimales :
1. Réduire progressivement la température à 10-15°C
2. Réduire la lumière (pas d’éclairage additionnel, seulement lumière naturelle)
3. Réduire les apports en nutriments
4. Ne pas récolter pendant cette période
5. Au printemps, augmenter progressivement température et lumière
Méthode 2 : Stockage sous forme sèche
1. Récolter et sécher le plus complètement possible
2. Stocker à température ambiante, à l’abri de l’humidité et de la lumière
3. En ressemis au printemps, réhydrater progressivement dans du milieu frais
4. Laisser s’acclimater quelques jours avant de reprendre la production
Méthode 3 : Culture d’hivernage en serre
Si on a une serre, on peut maintenir la production réduite en hiver avec :
1. Serre chauffée (minimum 15°C)
2. Éclairage LEDadditionnel
3. Production réduite mais continue
Remarque importante :
La spiruline ne craint pas le froid (<5°C) en tant que tel, mais elle arrête sa croissance. Une congélation prolongée peut la tuer.
A26) Formules d’Oligo-éléments
Solution d’oligo-éléments pour 1 litre de milieu de culture :
Recette A (formule simple) :
À ajouter pour 1 liter de milieu :
| Composant | Masse (mg) |
|---|---|
| FeCl3·6H2O (chlorure de fer III) | 8 |
| MnCl2·4H2O (chlorure de manganèse) | 4 |
| ZnCl2 (chlorure de zinc) | 3 |
| CuSO4·5H2O (sulfate de cuivre) | 2 |
| CoCl2·6H2O (chlorure de cobalt) | 0,5 |
| H3BO3 (acide borique) | 2,5 |
| Na2MoO4·2H2O (molybdate de sodium) | 0,5 |
Préparation :
1. Dissoudre chaque sel dans un peu d’eau distillée
2. Bien mélanger
3. Diluer le tout dans 1 litre de milieu
4. Bien homogénéiser
Recette B (formule avec EDTA pour meilleure biodisponibilité) :
Pour 1 litre de milieu :
| Composant | Masse (mg) |
|---|---|
| Na2EDTA·2H2O (EDTA disodique) | 80 |
| FeSO4·7H2O (sulfate de fer) | 140 |
| MnSO4·H2O (sulfate de manganèse) | 20 |
| ZnSO4·7H2O (sulfate de zinc) | 30 |
| CuSO4·5H2O (sulfate de cuivre) | 2 |
| CoCl2·6H2O (chlorure de cobalt) | 2 |
| H3BO3 (acide borique) | 50 |
| Na2MoO4·2H2O (molybdate de sodium) | 1 |
Remarques :
– La recette B avec EDTA offre une meilleure disponibilité des éléments
– EDTA est un complexant qui chélate les métaux et améliore l’absorption par la spiruline
– Les deux recettes donnent de bons résultats en pratique
A27) Modèles de Séchoirs
1. Séchoir solaire simple
Description :
– Cadre en bois avec film plastique transparent
– Plateau perforé pour poser la spiruline
– Aération naturelle
Avantages :
– Très bas coût (20-50€)
– Simple à construire
– Pas d’électricité
Inconvénients :
– Dépend du climat
– Séchage lent (2-3 jours)
– Risque de pluie ou d’insectes
2. Séchoir solaire ventilé
Description :
– Boîte isolée thermiquement
– Film plastique transparent sur le toit
– Petit ventilateur (batterie solaire) pour la circulation d’air
– Grilles empilables
Avantages :
– Meilleur contrôle
– Séchage plus rapide (18-24h)
– Protection contre les contaminants
– Pas d’électricité externe
Inconvénients :
– Coût plus élevé (100-300€)
– Maintenance du ventilateur
3. Séchoir électrique à air chaud
Description :
– Boîte thermiquement isolée
– Résistance électrique chauffante
– Ventilateur pour circulation d’air
– Thermostat pour contrôler la température
– Bac de collecte du condensat
Avantages :
– Très rapide (6-8 heures)
– Excellent contrôle de la température (35-45°C optimal)
– Protection complète
– Reproductible
Inconvénients :
– Coût plus élevé (500-2000€)
– Consommation d’électricité (1-2 kW)
4. Séchoir sous-vide
Description :
– Chambre sous vide partiel
– Chauffage doux (30-40°C)
– Récupération du condensat
Avantages :
– Température basse = meilleure conservation des vitamines
– Très efficace
Inconvénients :
– Très coûteux (3000€+)
– Complexe à utiliser
Choix recommandé pour petite production :
Le séchoir solaire ventilé ou le séchoir électrique simple offrent le meilleur compromis qualité/coût/performance.
A28) Projet semi-artisanal de 5 kg/jour
Objectif : Production de 5 kg/jour de spiruline sèche (soit environ 25 kg/jour de biomasse mouillée)
Dimensions du bassin :
– Bassin de 50 m² de surface (ex : 10 m x 5 m)
– Profondeur : 0,3 m
– Volume : 15 m³
– Charge volumique à 4 g/L : 60 kg de spiruline fraîche
Bassin de maturation :
– 5 m² pour décantation/clarification
– Profondeur : 0,5 m
Équipements :
– Aérateur mécanique : 10-20 kW
– Pompes (alimentation, vidange) : 2-3 kW
– Filtres (tambour rotatif, toile inox) : 1-2 kW
– Séchoir électrique : 3-5 kW
– Moulins, stockage : divers
Consommation d’eau :
Environ 50-100 L/kg de produit sec (soit 250-500 L/jour pour 5 kg)
Consommation d’électricité :
– Aération : 6-8 heures/jour (60-160 kWh/jour)
– Pompes : 4-6 heures/jour (20-30 kWh/jour)
– Filtration : 2-3 heures/jour (5-10 kWh/jour)
– Séchage : 10-12 heures/jour (30-60 kWh/jour)
– Total : 115-260 kWh/jour
Coûts annuels estimés :
| Poste | Coût annuel |
|---|---|
| Nutriments | 10 000€ |
| Électricité (0,15€/kWh) | 6 300€ |
| Eau | 500€ |
| Maintenance | 3 000€ |
| Main-d’œuvre | Variable |
| Amortissement du matériel | ~50 000€/5 ans = 10 000€ |
| TOTAL (sans main-d’œuvre) | ~30 000€/an |
Revenus estimés :
À 50€/kg en gros :
5 kg/jour × 350 jours/an × 50€/kg = 87 500€
Marge brute : 87 500€ – 30 000€ = 57 500€ (avant main-d’œuvre)
Remarques :
– Ces chiffres sont des estimations et peuvent varier significativement
– La main-d’œuvre est un coût important non inclus
– Meilleur rendement obtenu avec système d’aération adéquat
– Qualité et prix varient selon les marchés
A29) Check list pour démarrage de spiruline
Avant de commencer :
1. Déterminer les objectifs (hobby, petite vente, grande production)
2. Choisir le type de système (ouvert, semi-fermé, fermé)
3. Évaluer le climat local (température, ensoleillement)
4. Vérifier les ressources (eau, électricité, espace)
5. Rechercher et se former
Infrastructure et matériel :
[] Bassin de culture (dimensions selon objectifs)
[] Système d’aération (aérateur électrique ou paddle-wheel)
[] Pompes (alimentation, vidange)
[] Tuyauterie et connexions
[] Filtration (filtre tambour ou toile fine)
[] Séchoir (solaire ou électrique)
[] Moulins/broyeurs
[] Système de mesure (pH, température, salinité, OD)
[] Équipements de sécurité (gants, masques)
Produits chimiques :
[] Nitrate de sodium (NaNO3)
[] Phosphate (K2HPO4)
[] Sulfate de potassium (K2SO4)
[] Chlorure de sodium (NaCl)
[] Sulfate de magnésium (MgSO4)
[] Chlorure de calcium (CaCl2)
[] Chlorure de fer (FeCl3)
[] EDTA disodique
[] Bicarbonate de sodium (NaHCO3)
[] Carbonate de sodium (Na2CO3)
[] Oligo-éléments (divers sels)
Culture de démarrage :
[] Obtenir une culture de démarrage fiable (contact avec producteur, etc.)
[] Tester sa qualité (couleur, pureté, vigueur)
[] Prévoir un petit bassin de multiplication
Connaissances :
[] Lire ce manuel en entier
[] Pratiquer les mesures de base (pH, température)
[] Comprendre les principes de nutrition
[] Connaître les contaminants possibles
[] Savoir récolter et sécher correctement
Démarrage :
[] Préparer le milieu de culture
[] Inoculer le bassin
[] Vérifier le pH et la température
[] Laisser s’acclimater 2-3 jours
[] Commencer aération douce
[] Monitorer quotidiennement (pH, température, apparence)
Premiers jours :
[] Phase de latence (1-3 jours) : peu de changement visible
[] Phase exponentielle (3-7 jours) : croissance rapide
[] Phase stationnaire : stabilisation
[] Commencer légères récoltes après 2-3 semaines
A30) Spiruline humanitaire dans les PVD (par P. Ancel, mai 2004)
Introduction
La spiruline offre une solution prometteuse pour la malnutrition dans les pays en développement (PVD), particulièrement en zones tropicales et semi-arides.
Avantages spécifiques pour les PVD :
1. Production locale simple : Pas besoin de technologie sophistiquée
2. Coûts bas : Surtout si électricité minime
3. Nutrition : 60-70% protéines, riche en fer et vitamines
4. Disponibilité : Production toute l’année en zones chaudes
5. Acceptabilité culturelle : Facilement intégrable dans l’alimentation traditionnelle
Applications humanitaires :
1. Complément alimentaire pour enfants malnutris
Dosage : 2-3 g/jour pour enfant de 5-10 ans
Amélioration visible en 3-4 mois
Peut être mélangée à la farine locale
2. Enrichissement des repas collectifs
Écoles, orphelinats, hôpitaux
5-10 g/jour par personne
Améliore l’indice de masse corporelle
3. Prévention de l’anémie ferriprive
Riche en fer hautement biodisponible
Particulièrement utile pour femmes enceintes/allaitantes
Dosage : 3-5 g/jour
4. Soutien aux malades du VIH/SIDA
Renforce le système immunitaire
Facilement digestible
Dosage : 5-10 g/jour
Défis et solutions :
| Défi | Solution |
|---|---|
| Coûts initiaux du bassin | Sponsorships, micro-finance, partenariats |
| Stabilité de la culture | Formation adéquate, réseaux d’entraide |
| Contamination en zone chaude/humide | Hygiène stricte, faible salinité réduit risques |
| Acceptabilité locale | Éducation, recettes traditionnelles, sensibilisation |
| Distribution | Circuits courts, partenariats santé locaux |
Résultats probants :
Plusieurs projets pilotes en Afrique de l’Ouest et du Centre ont montré :
– Augmentation de poids : 2-4 kg en 6 mois chez enfants
– Augmentation de l’hémoglobine : 1-2 g/dL en 3 mois
– Amélioration de l’appétit et énergie
– Réduction des infections opportunistes
Recommandations :
1. Démarrer petit (petit bassin communautaire)
2. Former une équipe locale durable
3. Lier à un programme nutritionnel plus large
4. Évaluer régulièrement les résultats
5. Pérenniser par génération de revenus (petite vente locale)
A31) Adoucissement de l’eau
Problème :
Beaucoup d’eaux naturelles contiennent des sels de calcium et magnésium qui la rendent « dure ». Cela pose des problèmes dans la culture de spiruline :
1. Précipitation de calcaire (CaCO3)
2. Blocage des filtres
3. Perturbation du système tampon pH
Solutions d’adoucissement :
1. Résines échangeuses d’ions
Cartouches de résine commerciales
Principe : Na+ remplace Ca²+ et Mg²+
Avantages : Efficace, rapide
Inconvénients : Coûteux, régénération périodique
Coût : 100-300€ pour petit système
2. Chaux-soude (chimique)
Ajouter Ca(OH)2 puis Na2CO3
Précipite le Ca et Mg en bas du bac
Ensuite décanter
Avantages : Peu coûteux
Inconvénients : Lent, laisse résidus
Coût : 5-20€
3. Osmose inverse
Membranefine sous pression
Élimine tous les sels
Avantages : Très pur
Inconvénients : Très coûteux, gaspille 2/3 de l’eau
Coût : 500€ et plus
4. Distillation
Évaporation et condensation
Très pur
Coûteux en énergie
Coût énergétique important
5. EDTA (moins usuel)
Chélation des métaux
Ne réduit pas vraiment la « dureté »
Utilité mineure pour ce problème
Recommandation pratique :
Pour petite production :
– Si eau modérément dure : diluer avec eau de pluie
– Si eau très dure : utiliser résines échangeuses (investissement initial)
– Aération et décantation : méthode gratuite mais lente
Mesure de la dureté :
Dureté en °f (français) = (Ca²+ meq/L + Mg²+ meq/L) × 5
Échelle :
– < 7°f : eau très douce
– 7-15°f : eau douce
– 15-30°f : eau modérément dure
– > 30°f : eau très dure
NB 1 : Le Mg suit le même sort.
NB 2 : Il est fortement déconseillé de stocker l’eau épurée à la lumière car il y a risque de développement de microorganismes toxiques.